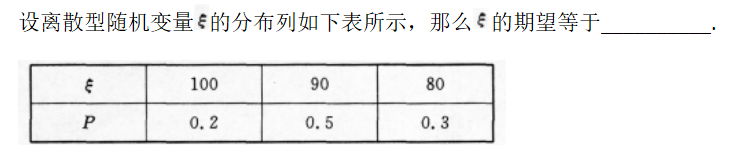
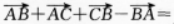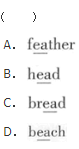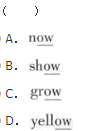下列各组溶液中,各溶质的物质的量浓度相同,其pH符合由小到大顺序的是( )
- A.KCl、HBr、HI
- B.HCl、H2SO4、H3PO4
- C.KOH、NaOH、Ca(OH)2
- D.HCl、CH3COOH、NH3·H2O
正确答案及解析
正确答案
D
解析
【解题指要】(1)pH由小到大的顺序就是酸性减弱、碱性增强的顺序.各组溶液中可以都是酸溶液或都是碱溶液,也可以是由酸溶液逐渐过渡到碱溶液. (2)HCl、H2SO4都是强酸,但HCl为一元强酸,H2SO4为二元强酸,所以当酸的物质的量浓度
相同时,H2SO4电离出的H+比HCl电离出的H+多1倍,即H2SO4溶液的酸性比HCl溶液强.所以B选项错误.
A选项中,KCl是强酸强碱盐,水溶液呈中性,而HBr、HI溶液均呈强酸性,所以不符合酸性减弱的顺序.
C选项中,KOH、NaOH溶液为强碱性,Ca(O