将0.1 mol/L的NaOH溶液20 mL与0.2 mol/L的CH3COOH溶液10 mL混合.混合后的溶液中,有关离子浓度间的关系正确的是( )
- A.C(Na+)>c(OH-)>c(H+)>c(CH3COO-)
- B.C(Na+)>c(OH-)>c(CH3COO-)>c(H+)
- C.C(Na+)>c(CH3COO-)>c(H+)>c(OH-)
- D.C(Na+)>c(CH3COO-)>c(OH-)>c(H+)
正确答案及解析
正确答案
D
解析
【解题指要】 溶液中含有NaOH和CH3COOH的物质的量分别为
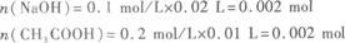
等物质的量的NaOH与CH3COOH恰好完全反应:

所以混合后的溶液可以看做是CH3COONa溶液,在此溶液中的离子有
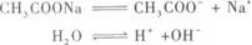
若不考虑水解,则有c(Na+)=c(CH3COO-);c(H+)=c(OH-).但事实是CH3COO-会发生水解:

由于水解反应消耗了CH3COO-且生成了OH-,所以c(Na+)>c(CH3COO-);C(OH-)>c(H+).由于水解程度一般都很低,所以c(CH3COO-)>c(OH-).
即:c(Na+)>c(CH3COO-)>c(OH-)>c(H+).